





























Dieser Hypertext soll Lernenden die vom NRW-G8-Kernlehrplan für die Sekundarstufe II der gymnasialen Oberstufe vorgeschriebenen biologischen Lerninhalte so verständlich erklären, dass sie sich den Stoff möglichst ohne Hilfe selbst erarbeiten oder ihn zumindest selbständig wiederholen können. Interessierten jüngeren Lernenden soll mein Lerntext als Selbstlernmaterial dienen, damit sie ihren Fähigkeiten entsprechend gefordert bleiben und schon in der Schulzeit ihre Studierfähigkeit entwickeln können.
Klickt man im Inhaltsverzeichnis auf die blauen Pfeile, so springt man innerhalb des Textes nach unten in das entsprechende Kapitel. Mit einem Klick auf die Kapitelüberschrift springt man vom Inhaltsverzeichnis direkt in ein ausführlicheres Kapitel eines anderen Textes.
 |
Die Sicherheitsbelehrung |
|---|---|
 |
Inhaltsfeld Biologie der Zelle |
 |
evolutionärer Wettkampf Zelle gegen Viren |
 |
Organellen |
 |
Der Aufbau einer tierischen Zelle |
 |
Lipide, die Zellmembran und Transmembran-Transport |
 |
Zellkerne mit Nukleoli und Zellkernhülle mit Kernporen |
 |
Chromosomen sind die Kochbücher des Lebens. |
 |
Alle Eukaryoten sind Endosymbiosen. |
 |
Die Bedeutung der Baupläne für alle Lebewesen |
 |
Übungsmodul zu den Fachbegriffen |
 |
Biopolymer-Fachbegriffe |
 |
von Aminosäuren zu Proteinen |
 |
die Strukturen von Nukleotiden und DNA |
 |
raues endoplasmatisches Retikulum |
 |
Membranfluss und Fließgleichgewicht |
 |
Mikrotubuli, Intermediärfilamente und Mikrofilamente bilden das Zytoskelett. |
 |
Zellzyklus mit DNA-Replikation und Mitose |
 |
Diffusion und Osmose |
 |
Erwartungshorizont |
 |
etwas Thermodynamik |
 |
Enzyme |
 |
2. Klausur |
 |
3. Klausur |
 |
|
 |
Unterrichtsvorhaben laut schulinternem Curriculum |
 |
Inhaltsfelder, inhaltliche Schwerpunkte, fachliche Kontexte und Basiskonzepte laut Kernlehrplan für die Erprobungsstufe |
 |
Wissen aktiv zu erarbeiten ist besser als sich passiv unterrichten zu lassen. |
 |
naturwissenschaftliche Grundlagen für das Verständnis der Biologie |
 |
Lernen mit Büchern |
Die Sicherheitsbelehrung
|
|---|
Hier findet Ihr die Sicherheitsbelehrung für Biologie-Räume.
Inhaltsfeld Biologie der Zelle
|
|---|
Was in der Jahrgangsstufe 10 (Einführungsphase) laut Kernlehrplan inhaltlich zum Inhaltsfeld Biologie der Zelle vermittelt werden soll, erklärt auch mein Lerntext Zellbiologie.
evolutionärer Wettkampf Zelle gegen Viren
|
|---|
Wir sahen und diskutierten eine Animation des Abwehrkampfes einer Zelle gegen Adenoviren, die sich in ihr zu vermehren versuchen. Man kann diese Dokumentation immer wieder im Fernsehen, aber auch jederzeit hier und hier im World Wide Web sehen.
Damit sich alle Lernenden voll auf die einmaligen Bilder konzentrieren können, habe ich den Inhalt des Films in einer eigenen Dokumentation zusammengefasst.
Anhand dieses Films besprachen wir wichtige Prinzipien der Biologie:
Organellen
|
|---|
Was wir über Organellen eukaryotischer Zellen erarbeitet haben, findet man im Lerntext Organellen.
Der Aufbau einer tierischen Zelle
|
|---|
Den im Unterricht erarbeiteten Aufbau einer tierischen Zelle findet man im Lerntext Organellen.
Lipide, die Zellmembran und Transmembran-Transport
|
|---|
In eigenen Lerntexten findet man Informationen zu den im Unterricht behandelten Themen Lipide, die Zellmembran und Transmembran-Transport.
Zellkerne mit Nukleoli und Zellkernhülle mit Kernporen
|
|---|
Die Themen Zellkerne (Nukleus) eukaryotischer Zellen, Nukleoli, Zellkernhülle und Kernporen erarbeiteten wir uns mit dem Lerntext Organellen:
Chromosomen sind die Kochbücher des Lebens.
|
|---|
Mit dem Lerntext Genetik erarbeiteten wir uns die Themen:
Alle Eukaryoten sind Endosymbiosen.
|
|---|
Informationen zur Endosymbionten-Theorie gibt es verteilt auf zwei Texte:
Die Bedeutung der Baupläne für alle Lebewesen
|
|---|
Mit dem Lerntext Genetik erarbeiteten wir uns die Themen:
Übungsmodul zu den Fachbegriffen
|
|---|
Ein Aufgabenmodul soll die Arbeit mit Material im Sinne einer Klausur einüben. Die Aufgaben für die selbständige Erarbeitung befinden sich im Übungsmodul Fachbegriffe. Die Informationen sollen in unserem Biologiebuch gefunden werden.
Biopolymer-Fachbegriffe
|
|---|
Eine Tabelle mit Biopolymer-Fachbegriffen findet man im Lerntext Biomoleküle.
In den folgenden Kapiteln werden die Peptide und die Nukleinsäuren näher betrachtet.
von Aminosäuren zu Proteinen
|
|---|
Mit dem Lerntext Biomoleküle erarbeiteten wir uns die Themen:
die Strukturen von Nukleotiden und DNA
|
|---|
Ebenfalls mit dem Lerntext Biomoleküle erarbeiteten wir uns die Themen:
raues endoplasmatisches Retikulum
|
|---|
Informationen zum rauen endoplasmatischen Retikulum der eukaryotischen Zellen findet man im Lerntext Organellen.
Membranfluss und Fließgleichgewicht
|
|---|
Informationen zu Membranfluss und Fließgleichgewicht findet man im Lerntext Membranfluss:
Mikrotubuli, Intermediärfilamente und Mikrofilamente bilden das Zytoskelett.
|
|---|
Informtationen über das aus Mikrotubuli, Intermediärfilamenten und Mikrofilamenten bestehende Zytoskelett gibt es im Lerntext Zellbiologie.
Zellzyklus mit DNA-Replikation und Mitose
|
|---|
Informationen zu Zellzyklus mit DNA-Replikation und Mitose findet man im Lerntext Lerntext Zellbiologie:
Diffusion und Osmose
|
|---|
Zur Erarbeitung und Wiederholung dieses Themas nutzen wir den Lerntext Diffusion und Osmose
Erwartungshorizont
|
|---|
Den Erwartungshorizont für die Klausur findet Ihr hier.
etwas Thermodynamik
|
|---|
Verglichen mit den Geschwindigkeiten chemischer Reaktionen ändern sich Temperatur und Druck in Zellen nur langsam. Man kann also bei den unzähligen, in lebenden Zellen ablaufenden chemischen Reaktionen davon ausgehen, dass Temperatur und Druck konstant bleiben. Unter diesen Umständen lässt sich mit folgender, relativ einfacher Gleichung ermitteln, ob eine chemische Reaktion spontan abläuft:
ΔG = ΔH - T · ΔS
G steht für die freie Energie eines Systems (z.B.: der an einer chemischen Reaktion besteiligten Edukte und Produkte). Die absolute Größe dieser freien Energie kann nicht bestimmt werden, sondern lediglich deren Änderungen ΔG.
H steht für die innere Energie (die gesamte für thermodynamische Umwandlungsprozesse zur Verfügung stehende Energie) des Systems (der an einer chemischen Reaktion besteiligten Stoffe). Die absolute Größe dieser inneren Energie kann nicht bestimmt werden, sondern lediglich deren Änderungen ΔH. Durch den Austausch von Wärme oder Arbeit kann sich die innere Energie eines Systems ändern.
S steht für die Entropie, also die molekulare Unordnung. T steht für die absolute Temperatur (in Kelvin) und Δ für eine Änderung.
Ist die Änderung der freien Energie ΔG negativ, dann kann eine chemische Reaktion spontan/freiwillig, also ohne Energiezufuhr von außen ablaufen. Solche chemischen Reaktionen nennt man exergonisch. Der Grund kann eine Abnahme der inneren Energie sein, also ein negatives ΔH. Chemische Reaktionen können aber auch angetrieben werden durch eine Zunahme der Entropie (Die Temperatur T bleibt ja praktisch konstant.). Im Gegensatz zur Darstellung unseres Buches laufen auch endergonische Prozesse laufen spontan/freiwillig ab, obwohl es dazu einer Energiezufuhr bedarf. Wäre es nicht so, dann könnten die meisten chemischen Reaktionen immer nur in eine Richtung ablaufen und eine Rückreaktion wäre unmöglich. Ist die Hinreaktion exergonisch und die Rückreaktion entsprechend endergonisch, dann gibt es im Gleichgewichtszustand mehr Produkte als Edukte, weil die Hinreaktion wahrscheinlicher als die Rückreaktion ist.
Exergonische chemische Reaktionen verwandeln zunächst Edukte (Ausgangsstoffe) in Produkte. Nehmen aber die Konzentrationen der Produkte zu und ist die chemische Reaktion reversibel (Das sind fast alle chemischen Reaktionen.), dann kommt es zu einer immer umfangreicheren Rückreaktion, bis sich bei irgendeinem Verhältnis von Edukten zu Produkten ein Gleichgewicht einstellt. Und weil in lebenden Zellen ständig Edukte nachgeliefert und Produkte verbraucht oder abtransportiert werden, bilden auch die chemischen Reaktionen in lebenden Zellen Fließgleichgewichte.
Enzyme
|
|---|
Wir haben unsere Buchseiten 69-71 als Material im Sinne einer Klausur genutzt, um die wesentlichen darin enthaltenen Informationen selbständig zusammenzufassen:
Enzyme sind von Lebewesen produzierte Katalysatoren und heißen deshalb auch Biokatalysatoren. Enzyme beschleunigen und lenken chemische Reaktionen. Dadurch können chemische Reaktionen bis zu 1012 mal schneller ablaufen. Das entspricht ungefähr der Beschleunigung einer Schnecke auf Lichtgeschwindigkeit.
Entscheidend ist das im Verlauf der Evolution perfektionierte aktive Zentrum eines Enzyms. Das aktive Zentrum bindet das Substrat nach dem Schlüssel-Schloss-Prinzip. Beide bilden in einer reversiblen Gleichgewichtsreaktion einen Enzym-Substrat-Komplex. Dabei verändern Enzym und Substrat ihre Formen so, dass das Substrat die gewünschte chemische Reaktion besser ausführen kann. Die Konformationen von Enzym und Substrat passen sich aneinander an und die Verbiegung des Substrates überführt es in einen energiereicheren und reaktionsfreudigeren Übergangszustand.
Nach einer chemischen Reaktion hat das Enzym wieder seine ursprüngliche Form, während die Substrate in die Produkte verwandelt wurden. Ein Beispiel dafür ist die Reaktion von Glucose und ATP zu ADP und Glucose-6-Phosphat.
Enzyme katalysieren die Hin- und auch die Rückreaktionen, sodass sich Gleichgewichte zwischen Substraten und Produkten einstellen. Dieses Gleichgewicht wird von Enzymen nicht beeinflusst.
Nicht wirklich erklärt hat unser Buch die Begriffe Cosubstrate, Cofaktoren und Coenzyme. Wir erarbeiten uns das mit dem Kapitel Cofaktoren in meinem Lerntext Stoffwechselphysiologie.
2. Klausur
|
|---|
Themen der 2. Klausur waren Diffusion, Osmose und Enzyme.
Richtige Lösungen findet Ihr hier.
3. Klausur
|
|---|
Themen der 3. Klausur waren Einfluss der Temperatur auf die Enzymkatalyse, Einfluss des pH-Wertes auf die Enzymkatalyse und Aktivierung und Hemmung enzymatischer Reaktionen.
Richtige Lösungen findet Ihr hier.
Was wir über Enzyme und ihre Regulation wissen sollten, steht zusammengefasst im Lerntext Stoffwechselphysiologie (zuletzt überarbeitet am 6.5.2017). Speziell für diese Klausur (9.6.) findet Ihr darin vor allem die Kurven zur Abhängigkeit der Enzym-Aktivität von Temperatur und pH-Wert sowie die Zeichnungen zur Regulation der Enzym-Aktivität. Zusätzlich empfehle ich zur Vorbereitung auf unsere 3. Klausur die Wiederholung der Antworten der Lernmodule zu den Buchseiten 72-77. vor. In den folgenden Abschnitten habe ich die inhaltlich klausurrelevanten Antworten dieser Lernmodule zusammengefasst. Das eigenständige Beantworten der Aufgaben in den Lernmodulen ist trotzdem wichtig für die Vorbereitung auf die Klausur, weil man damit das Verstehen von Aufgaben mit ihren Operatoren sowie das wirklich schwierige Formulieren von Antworten übt. Mit der im Unterricht leider oft praktizierten Gruppenarbeit, Abschreiben oder Auslassen von Aufgaben beraubt man sich selbst des Erwerbs wichtiger Kompetenzen. Der Lehrer sollte nicht der Einzige sein, der die Aufgaben selbständig, gründlich und vollständig löst.
Einige Definitionen zum besseren Verständnis:
Das folgende animierte gif wurde anonym als public domain frei verfügbar gemacht und stellt die Succinat-Dehydrogenase mit ihren Cofaktoren dar.
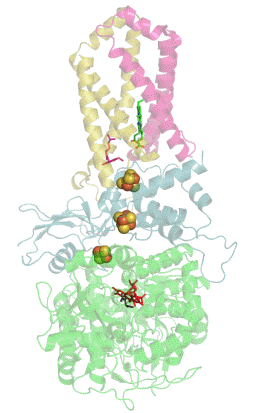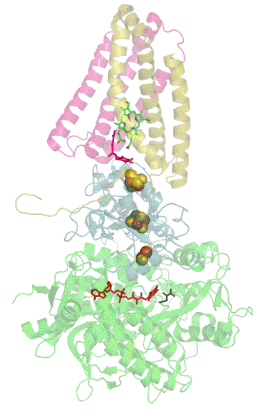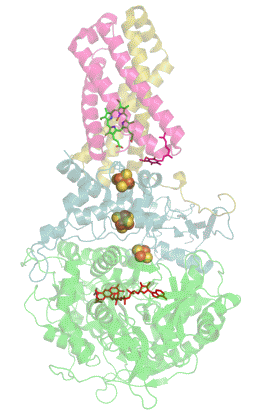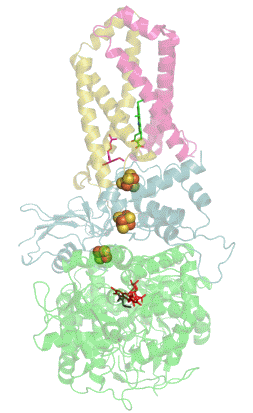
Im aktiven Zentrum eines Enzyms bilden sich Wasserstoffbrückenbindungen zwischen Substrat bzw. Cosubstrat und bestimmten Aminosäuren des Enzyms. Diese Wasserstoffbrückenbindungen verändern die chemischen Eigenschaften von Substrat und Cosubstrat und erleichtern dadurch die chemische Reaktion.
Veränderte Konzentrationen oder Aktivitäten von Enzymen können auf bestimmte Krankheiten hinweisen (z.B.: Tumormarker).
Die Aktivitäten von Enzymen lassen sich z.B. indirekt dadurch bestimmen, dass man in Lösungen die Änderungen bestimmter optischer Eigenschaften bestimmt, die von den Mengenverhältnissen zwischen Edukten und Produkten abhängen. Dann kann man relative Enzymaktivitäten bestimmen, indem man bei unterschiedlichen Substrat-Konzentrationen die Geschwindigkeiten der Produktproduktion ohne und mit bestimmten Enzym-Konzentrationen vergleicht.
Verdoppelt oder verdreifacht man bei einer chemischen Reaktion die Konzentrationen der Edukte, dann verdoppelt oder verdreifacht sich auch die Reaktionsgeschwindigkeit. Die Aussage des Buches ist falsch, weil die Erhöhung der Konzentration nur eines Edukts zu einem Sättigungseffekt führen könnte.
Bei von Enzymen katalysierten chemischen Reaktionen ist die Reaktionsgeschwindigkeit sehr viel höher, hängt aber auch von der Enzym-Konzentration ab. Mit zunehmender Substrat-Konzentration kommt es immer häufiger vor, dass Substrat-Moleküle statt eines freien Enzyms einen Enzym-Substrat-Komplex antreffen und deshalb auf ein freies Enzym warten müssen. Darum wirken sich Steigerungen der Substrat-Konzentration immer weniger stark und irgendwann gar nicht mehr aus. Zeichnet man in einem Diagramm die Funktion der Reaktionsgeschwindigkeit in Abhängigkeit von der Substrat-Konzentration, dann erhält man eine sich zunehmend abflachende Sättigungskurve. Aus ihr kann man für eine gegebene Enzym-Konzentration leicht die maximale und die halbmaximale Reaktionsgeschwindigkeit ablesen.
Bei der Maximalgeschwindigkeit stecken praktisch alle Enzyme ständig in Enzym-Substrat-Komplexen, sodass eine weitere Steigerung der Substrat-Konzentration nichts mehr bringt. Weil sich die Sättigungskurve immer langsamer dem Maximum nähert, lässt sich die für die Maximalgeschwindigkeit erforderliche Substrat-Konzentration nicht leicht ablesen. Darum liest man aus dem Diagramm die Substrat-Konzentration bei halbmaximaler Reaktionsgeschwindigkeit ab, nennt diesen Wert Michaelis-Konstante und charakterisiert mit ihr die Geschwindigkeit, mit der ein Enzym arbeiten kann.
Selbstverständlich sind auch die Reaktionsgeschwindigkeiten der Enzyme evolutionär durch zufällige Mutationen und natürliche Selektion optimiert.
In saurer Umgebung werden drei Aminosäuren im aktiven Zentrum der Hexokinase protoniert. Das bedeutet, dass ihre Carboxylgruppen jeweils ein Proton binden. Dadurch werden Wasserstoffbrückenbindungen zu Substrat und Cosubstrat aufgelöst und die Funktion des Enzyms beeinträchtigt.
Bei sehr niedrigen pH-Werten denaturieren viele Proteine. Denaturierung bedeutet Auflösung der Raumstruktur. Gemeint ist damit hauptsächlich die Tertiärstruktur. Es können aber auch Sekundärstrukturen und gegebenenfalls die Quartärstruktur beroffen sein. Die Primärstruktur ist sehr stabil und wird weder durch Magensäure noch durch Kochen oder Braten zerstört.
Bauchspeichel enthält verschiedene Verdauungsenzyme in einer neutralisierenden Flüssigkeit. Da sie den sauren Magensaft neutralisiert, muss sie basisch sein.
Proteine bestehen aus Aminosäuren, von denen es in menschlichen Proteinen 20 verschiedene gibt. Einige von ihnen reagieren bei niedrigen pH-Werten als Basen und nehmen positive elektrische Ladungen an, die dann von anderen positiven Ladungen im selben Protein abgestoßen werden und dadurch die räumliche Struktur des Proteins auflockern. Säure-resistente Varianten eines Proteins können sich daher durch den Austausch solcher Proteine entwickeln. Dazu müssen nur einzelne Nukleotide in den entsprechenden Genen durch zufällige Mutationen ausgetauscht werden.
Weil höhere Temperaturen im Durchschnitt höhere kinetische Energien der Teilchen bedeuten, erhöhen sie die Wahrscheinlichkeit, dass Substrate genau in der richtigen Orientierung auf das aktive Zentrum eines Enzyms treffen. Enzyme verlieren aber oberhalb ihrer Temperaturoptima ihre Funktionsfähigkeit, weil die Funktion von der Form abhängt und weil übermäßige kinetische Energien der Atome zuerst die Tertiärstruktur und später auch noch die Sekundärstrukturen eines Enzyms zerstören.
Im Verlauf ihrer Evolution haben verschiedene Spezies ihre Enzyme an unterschiedliche Temperaturbereiche angepasst. Trotzdem sehen die Kurven praktisch gleich aus, wenn man die Enzym-Aktivitäten in Abhängigkeit von der Temperatur zeichnet. Das liegt daran, dass relativ unabhängig vom jeweiligen Temperaturbereich die RGT-Regel gilt und die Denaturierung oberhalb des Temperaturoptimums die gleiche Folge für die Funktionsfähigkeiten der Enzyme haben. Die Abbildung 1 zeigt, dass Enzyme aufgrund unterschiedlicher Primärstrukturen unterschiedlich auf verschiedene pH-Werte reagieren.
Punktmutationen in ihren Genen können zu hitzestabilen Varianten von Proteinen führen, weil dadurch an vielen Stellen Aminosäuren so ausgetauscht werden, dass sich benachbarte Aminosäuren beispielsweise durch unterschiedliche elektrische Ladungen stärker anziehen.
Im Stoffwechsel eines Lebewesens ist oft das Produkt einer chemischen Reaktion gleichzeitig das Substrat eines oder mehrerer weiterer Enzyme. So katalysieren Enzyme ganze Ketten (Stoffwechselwege) oder Netzwerke von chemischen Reaktionen. Dabei ist es erforderlich, das jedes Enzym sein Substrat in der benötigten Menge erhält. Andererseits könnte die Überproduktion eines Zwischenproduktes zu Verschwendung oder gar zur Anhäufung giftiger Stoffe führen. Hinzu kommt, dass sich in Lebewesen der Bedarf an bestimmten Reaktionsprodukten rasch ändern kann. Deshalb müssen Stoffwechselwege längerfristig, mittelfristig und manchmal auch sehr schnell aktiviert oder gehemmt werden können. Dazu können Gene inaktiviert und die Produktion nicht mehr gebrauchter Enzyme gestoppt werden, aber am schnellsten wirksam ist die Hemmung der bereits vorhandenen Enzyme.
Es gibt Stoffwechsel-Krankheiten, bei denen Enzyme zuviele oder fehlerhafte Produkte erzeugen. Dann kann es möglich sein, die Stoffwechsel-Krankheit zu lindern, indem man das störende Enzym mit einem passenden Inhibitor inaktiviert. Solch ein Inhibitor ist dann pharmakologisch wirksam. Damit er pharmakologisch wirksam sein kann, muss ein Inhibitor wie ein Schlüssel ins aktive Zentrum oder in eine andere (allosterische) Bindungsstelle des zu inhibierenden Enzyms passen und mit dessen Form auch seine Funktion bzw. Aktivität ändern.
Der Sinn der negativen Rückkopplung ist die automatische Regulation von Stoffwechselwegen. Regulation ist notwendig, weil sonst an vielen Stellen des Stoffwechsels Überschüsse produziert würden. Überproduktion von Stoffen würde nicht nur Verschwendung von Nährstoffen bedeuten, sondern könnte Zellen auch vergiften oder ihre Differenzierung stören. Der Mechanismus der Regulation durch negative Rückkopplung funktioniert so, dass ein Reaktionsprodukt an ein möglichst weit vorne (idealerweise am Anfang) in der Produktionskette seiner eigenen Herstellung wirkendes Enzym bindet. Durch diese Bindung wird die Form des Enzyms derart verändert, dass es weniger aktiv ist. So wird automatisch die Produktion des Stoffwechselendproduktes und gegebenenfalls der Zwischenprodukte reduziert (Endprodukthemmung, nicht zu verwechseln mit der Endproduktrepression).
Bei der kompetitiven Hemmung bindet ein Molekül (Inhibitor) an das aktive Zentrum eines Enzyms und blockiert damit das aktive Zentrum für das Substrat. Bei der allosterischen Hemmung bindet der Hemmstoff an einer anderen Bindungensstelle des Enzyms. Der Inhibitor kann das Produkt des Enzyms sein oder ein Produkt eines anderen Enzyms weiter hinten in einem Stoffwechselweg. Ein kompetitiver Inhibitor kann aber auch ein auf anderem Wege produziertes Molekül sein, das in das aktive Zentrum passt. Der Sinn kann eine negative Rückkopplung sein, aber auch die Unterdrückung eines alternativen Stoffwechselweges.
Im folgenden Diagramm zeigt die grüne Kurve, dass die Reaktionsgeschwindigkeit eines Enzyms umso größer ist, je höher die Konzentration des Substrats ist. Man sieht aber auch einen zunehmenden Sättigungseffekt, weil die Substrate immer häufiger auf schon besetzte Enzyme treffen. Die blaue Kurve zeigt, dass die Zunahme der Reaktionsgeschwindigkeit mit zunehmender Substrat-Konzentration langsamer erfolgt, wenn die Lösung außer dem Enzym und seinem Substrat auch noch einen kompetitiven Inhibitor enthält. Das liegt daran, dass Inhibitor und Substrat um die Bindung am aktiven Zentrum des Enzyms konkurrieren (Konkurrenz = Competition). Das Erreichen der maximalen Reaktionsgeschwindigkeit wird aber praktisch nicht verhindert, wenn die Konzentration des Substrats um Größenordnungen höher als die des kompetitive Inhibitors ist.
| Diagramm der kompetitiven Hemmung |
|---|
| Dieses Diagramm vergleicht für eine Enzym-Reaktion die Reaktionsgeschwindigkeiten ohne Inhibitor und mit reversibler oder irreversibler kompetitiver Hemmung. |
Unterrichtsvorhaben laut schulinternem Curriculum
|
|---|
Stand: Juli 2015
Realistischer als der NRW-G8-Kernlehrplan für die Sekundarstufe II der gymnasialen Oberstufe geht unser schulinternes Curriculum davon aus, dass nur wenige Lernende in der Einführungsphase noch wirklich wissen, was sie einmal in der Sekundarstufe 1 gelernt haben. Nicht nur die von einer Realschule auf das Gymnasium gewechselten Lernenden haben außerdem in der Sekundarstufe I nicht alles lernen können, was die gymnasialen Lehrpläne verlangen. Leider fehlt uns aber die Zeit, in der Einführungsphase den gesamten Stoff der Sekundarstufe 1 noch einmal gemeinsam zu wiederholen. Deshalb hat die Fachkonferenz Biologie beschlossen, dass die Lernenden das theoretisch von ihnen zu erwartende Vorwissen in der Einführungsphase weitgehend selbständig auffrischen bzw. ergänzen sollen. Nicht benotete Tests oder Selbstevaluationsbögen könnten aufzeigen, wo die jeweiligen Wissenslücken sind. Ich werde stattdessen immer wieder während der Erarbeitung neuer Lerninhalte auf den Stoff der Sekundarstufe 1 zu sprechen kommen.
Unser schulinternes Curriculum sieht vor, dass den Lernenden die Auffrischung wichtigen Vowissens durch einfache, kurze Texte erleichtert werden soll. Ich stelle solche Texte auf meinen Internetseiten zur Verfügung. Man findet sie insbesondere in der Navigationsleiste meiner Biologieseiten als buchunabhängige Lerntexte, aber auch in den Lerntexten, die ich an anderen Gymnasien für meine Klassen und Kurse der Sekundarstufe I erstellt habe. Eine Besonderheit meiner Lerntexte ist, dass darin die meisten Fachbegriffe mit meinem Glossar verlinkt sind, in dem ich fast 2000 biologische Fachbegriffe verständlich zu erklären versuche. Lernende sollten heute aber auch immer bedenken, dass man im World Wide Web eine große Vielfalt von teilweise sehr gutem Biologie-Selbstlernmaterial findet. Oft lohnt es sich, Suchbegriffe direkt bei Youtube einzugeben oder nach Google-Suchen die Liste der gefundenen Videos anzuklicken.
Inhaltsfelder, inhaltliche Schwerpunkte, fachliche Kontexte und Basiskonzepte laut Kernlehrplan für die Erprobungsstufe
|
|---|
Welche inhaltlichen Schwerpunkte wir uns im Fach Biologie in der Erprobungsstufe erarbeiten sollen, gibt der Kernlehrplan Biologie verbindlich vor. Ein gelegentlicher Blick auf die darin genannten Themen kann daher nicht schaden.
Wissen aktiv zu erarbeiten ist besser als sich passiv unterrichten zu lassen.
|
|---|
In den Biologie-Kursen der Jahrgangsstufe 10 kommen Schülerinnen und Schüler aus verschiedenen Klassen zusammen, die in den vorangegangenen Jahren nicht alle gleich viel gelernt und auch nicht unbedingt den gleichen Stoff im Unterricht behandelt haben. Wer jetzt im Unterricht Lücken in seinem Vorwissen bemerkt, kann Hilfe zum Selberlernen in meinem buchunabhängigen Lerntexten sowie in den Dokumentationen finden. Zum Thema Zellbiologie kann man aber auch die im Lerntext Zellbiologie gesammelten Links zu externen Quellen nutzen.
Hintergrund-Informationen dazu liefert mein Lerntext Lernen.
naturwissenschaftliche Grundlagen für das Verständnis der Biologie
|
|---|
Zur Erklärung naturwissenschaftlicher Grundlagen für das Verständnis der Biologie gibt es die Lerntexte:
Lernen mit Büchern
|
|---|
Mit Büchern kann man lernen, indem man sie einfach liest oder wichtige Aussagen markiert oder nur durch Wiederholung Erlernbares aufschreibt oder über Inhalte diskutiert. Schlichtes Lesen und auch bloßes Diskutieren reichen allerdings bei Biologiebüchern nicht aus. Man muss auch mit zusätzlichen Quellen unzählige Begriffe klären und durch mehrfache Wiederholung ähnlich wie Vokabeln auswendiglernen. Um beim Wiederholen nicht zu viel lesen zu müssen, sollte man aus einem Buch mit eigenen Worten so viel wie nötig, aber auch so wenig wie möglich herausschreiben. Dann kann man täglich das schon Gelernte wiederholen, bevor man mit der Erarbeitung weiteren Wissens fortfährt. Daneben geht es natürlich immer auch um die Kunst des eleganten, präzisen und unmissverständlichen Formulierens. Und sogar noch wichtiger ist mir als Naturwissenschaftler die Gewöhnung an das unbequeme naturwissenschaftliche Denken.
Roland Heynkes, CC BY-NC-SA 4.0